Peptidă
Peptidele sunt lanțuri scurte de aminoacizi legați prin legături peptidice. O polipeptidă este un lanț peptidic mai lung, continuu, neramificat. Polipeptidele care au o masă moleculară de 10.000 Da sau mai mult se numesc proteine. Lanțurile de mai puțin de douăzeci de aminoacizi sunt numite oligopeptide și includ dipeptide, tripeptide și tetrapeptide.
Peptidele se încadrează în clasele chimice largi de polimeri și oligomeri biologici, alături de acizi nucleici, oligozaharide, polizaharide și altele.
Proteinele constau din una sau mai multe polipeptide aranjate într-un mod biologic funcțional, adesea legate de liganzi cum ar fi coenzime și cofactori, de altă proteină sau altă macromoleculă, cum ar fi ADN sau ARN, sau de ansambluri macromoleculare complexe.
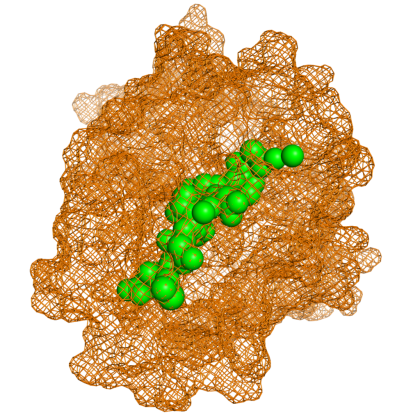
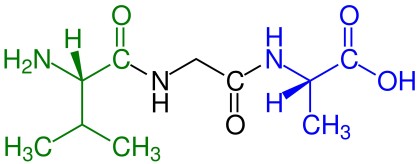
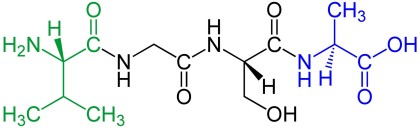
Aminoacizii care au fost încorporați în peptide sunt numiți reziduuri. O moleculă de apă este eliberată în timpul formării fiecărei legături amidice. Toate peptidele, cu excepția peptidelor ciclice, au un rest N-terminal (grup amină) și C-terminal (grup carboxil) la capătul peptidei (așa cum se arată pentru tetrapeptida din imagine).
Clasificare
Există numeroase tipuri de peptide care au fost clasificate în funcție de sursele și funcțiile lor. Conform Manualului de peptide biologic active, unele grupuri de peptide includ peptide de plante, peptide bacteriene/antibiotice, peptide fungice, peptide de nevertebrate, peptide de amfibieni/piele, peptide veninoase, peptide canceroase/anticanceroase, peptide de vaccin, peptide imune/inflamatorii, creier. peptide, peptide endocrine, peptide digestive, peptide gastrointestinale, peptide cardiovasculare, peptide renale, peptide respiratorii, peptide opioide, peptide neurotrofice și peptide hemato-encefalică.
Unele peptide ribozomale sunt supuse proteolizei. Acestea funcționează, de obicei în organismele superioare, ca hormoni și molecule de semnalizare. Unii microbi produc peptide ca antibiotice, cum ar fi microcinele și bacteriocinele.
Peptidele au frecvent modificări post-translaționale, cum ar fi fosforilarea, hidroxilarea, sulfonarea, palmitoilarea, glicozilarea și formarea disulfurei. În general, peptidele sunt liniare, deși au fost observate structuri lariate. Mai multe manipulări exotice apar, cum ar fi racemizarea L-aminoacizilor la D-aminoacizi în veninul de ornitorinc.
Peptidele nonribozomale sunt asamblate de enzime, nu de ribozom. O peptidă neribozomală comună este glutationul, o componentă a apărării antioxidante a majorității organismelor aerobe. Alte peptide nonribozomale sunt cele mai frecvente în organismele unicelulare, plante și ciuperci și sunt sintetizate de complexe enzimatice modulare numite sintetaze peptidice nonribozomale.
Aceste complexe sunt adesea dispuse într-un mod similar și pot conține multe module diferite pentru a efectua un set divers de manipulări chimice asupra produsului în curs de dezvoltare. Aceste peptide sunt adesea ciclice și pot avea structuri ciclice foarte complexe, deși peptidele liniare nonribozomale sunt, de asemenea, comune. Deoarece sistemul este strâns legat de mașinile de construcție a acizilor grași și polichetidelor, se găsesc adesea compuși hibrizi. Prezența oxazolilor sau tiazolilor indică adesea că compusul a fost sintetizat în acest mod.
Peptonele sunt derivate din laptele animal sau din carne digerată prin proteoliză. Pe lângă faptul că conține peptide mici, materialul rezultat include grăsimi, metale, săruri, vitamine și mulți alți compuși biologici. Peptonele sunt folosite în mediile nutritive pentru creșterea bacteriilor și ciupercilor.
Fragmentele de peptide se referă la fragmente de proteine care sunt utilizate pentru a identifica sau cuantifica proteina sursă. Adesea acestea sunt produse ale degradării enzimatice efectuate în laborator pe o probă controlată, dar pot fi și probe medico-legale sau paleontologice care au fost degradate prin efecte naturale.
Sinteză chimică
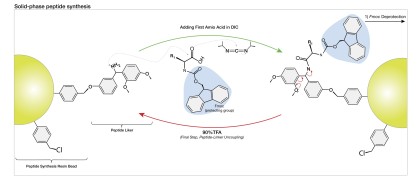
În chimia organică, sinteza peptidelor este producerea de peptide, compuși în care mai mulți aminoacizi sunt legați prin legături amidice, cunoscute și sub denumirea de legături peptidice. Peptidele sunt sintetizate chimic prin reacția de condensare a grupării carboxil a unui aminoacid la gruparea amino a altuia. Strategiile de grup de protecție sunt de obicei necesare pentru a preveni reacțiile secundare nedorite cu diferitele lanțuri laterale de aminoacizi. Sinteza chimică a peptidei începe cel mai frecvent la capătul carboxil al peptidei (capătul C-terminal) și continuă spre capătul amino-terminal (capitul N-terminal). Biosinteza proteinelor (peptide lungi) în organismele vii are loc în direcția opusă.
Sinteza chimică a peptidelor poate fi efectuată folosind tehnici clasice în fază de soluție, deși acestea au fost înlocuite în majoritatea setărilor de cercetare și dezvoltare prin metode în fază solidă. Sinteza în fază soluție își păstrează utilitatea în producția pe scară largă de peptide în scopuri industriale.
Sinteza chimică facilitează producerea de peptide care sunt greu de exprimat în bacterii, încorporarea de aminoacizi nenaturali, modificarea scheletului peptidic/proteic și sinteza proteinelor D, care constau din aminoacizi D.
Interacțiuni proteină-peptidă
Peptidele pot realiza interacțiuni cu proteinele și alte macromolecule. Ei sunt responsabili pentru mai multe funcții importante în celulele umane, cum ar fi semnalizarea celulară și acționează ca modulatori imunitari. Într-adevăr, studiile au raportat că 15-40% din toate interacțiunile proteină-proteină din celulele umane sunt mediate de peptide. În plus, se estimează că cel puțin 10% din piața farmaceutică se bazează pe produse cu peptide.
Exemple de familii
Familiile de peptide din această secțiune sunt peptide ribozomale, de obicei cu activitate hormonală. Toate aceste peptide sunt sintetizate de celule ca „propeptide” sau „proproteine” mai lungi și trunchiate înainte de a ieși din celulă. Ele sunt eliberate în fluxul sanguin unde își îndeplinesc funcțiile de semnalizare.
Peptide antimicrobiene
- Familia Magainin
- Familia Cecropin
- Familia Cathelicidin
- Familia Defensin
Peptide de tahikinină
- Substanța P
- Kassinin
- Neurokinina A
- Eledoisin
- Neurokinina B
Peptide intestinale vasoactive
- VIP (peptidă intestinală vasoactivă; PHM27)
- PACAP Peptida de activare a adenilat-ciclazei hipofizare
- Peptida PHI 27 (peptidă histidină izoleucină 27)
- GHRH 1-24 (hormonul de eliberare a hormonului de creștere 1-24)
- Glucagon
- Secretina
Peptide înrudite cu polipeptidele pancreatice
- NPY (NeuroPeptide Y)
- PYY (peptidă YY)
- APP (polipeptidă pancreatică aviară)
- PPY polipeptidă pancreatică
Peptide opioide
- Peptide proopiomelanocortin (POMC).
- Pentapeptide de encefalină
- Peptide prodinorfine
Peptide calcitonine
- Calcitonina
- amilină
- AGG01
Peptide cu auto-asamblare
- Peptide scurte aromatice
- Peptide biomimetice
- Amfifile peptidice
- dendrimeri peptidici
Alte peptide
- Peptida natriuretică de tip B (BNP) - produsă în miocard și utilă în diagnosticul medical
- Lactotripeptide - Lactotripeptidele ar putea reduce tensiunea arterială, deși dovezile sunt mixte.
- Componente peptidice din medicina traditionala chineza Colla Corii Asini in hematopoieza
Terminologie
Lungime
Mai mulți termeni legați de peptide nu au definiții stricte ale lungimii și adesea există o suprapunere în utilizarea lor:
- O polipeptidă este un singur lanț liniar de mulți aminoacizi (orice lungime), ținut împreună prin legături amidice.
- O proteină constă din una sau mai multe polipeptide (cu o lungime mai mare de aproximativ 50 de aminoacizi).
- O oligopeptidă constă doar din câțiva aminoacizi (între doi și douăzeci).
Numărul de aminoacizi
Peptidele și proteinele sunt adesea descrise prin numărul de aminoacizi din lanțul lor, de ex. o proteină cu 158 de aminoacizi poate fi descrisă ca o „proteină lungă de 158 de aminoacizi”. Peptidele cu lungimi mai scurte specifice sunt denumite folosind prefixele multiplicatoare numerice IUPAC:
- O monopeptidă are un aminoacid.
- O dipeptidă are doi aminoacizi.
- O tripeptidă are trei aminoacizi.
- O tetrapeptidă are patru aminoacizi.
- O pentapeptidă are cinci aminoacizi. (de exemplu, encefalina).
- O hexapeptidă are șase aminoacizi. (de exemplu, angiotensina IV).
- O heptapeptidă are șapte aminoacizi. (de exemplu, spinorfina).
- O octapeptidă are opt aminoacizi (de exemplu, angiotensina II).
- O nonapeptidă are nouă aminoacizi (de exemplu, oxitocină).
- O decapeptidă are zece aminoacizi (de exemplu, hormonul de eliberare a gonadotropinei și angiotensina I).
- O undecapeptidă are unsprezece aminoacizi (de exemplu, substanța P).
Aceleași cuvinte sunt, de asemenea, folosite pentru a descrie un grup de reziduuri dintr-o polipeptidă mai mare.
Funcţie
- O neuropeptidă este o peptidă care este activă în asociere cu țesutul neural.
- O lipopeptidă este o peptidă care are o lipidă conectată la ea, iar pepducinele sunt lipopeptide care interacționează cu GPCR.
- Un hormon peptidic este o peptidă care acționează ca un hormon.
- O proteoză este un amestec de peptide produs prin hidroliza proteinelor. Termenul este oarecum arhaic.
- Un agent peptidergic (sau medicament) este o substanță chimică care funcționează pentru a modula direct sistemele de peptide din organism sau creier. Un exemplu sunt opioidergicele, care sunt neuropeptidergice.
- O peptidă care pătrunde în celule este o peptidă capabilă să pătrundă în membrana celulară.